Урок па тэме: “Рэакцыі іоннага абмену. Умовы працякання
рэакцый іоннага абмену.”. 8 клас
Прэзентацыя "Рэакцыі іоннага абмену. Умовы іх працякання"
В. М. Дзямчук, настаўнік хіміі дзяржаўнай установы адукацыі
“Любанская сярэдняя школа Лунінецкага раёна”
Мэты ўрока:
- арганізаваць дзейнасць вучняў для замацавання ведаў аб працэсах, што адбываюцца ў растворах электралітаў - рэакцыях іоннага абмену, выяўлення ўмоў, пры якіх іонныя рэакцыі працякаюць неабарачальна;
- прадоўжыць фарміраваць у вучняў ўменні састаўляць ураўненні рэакцый іоннага абмену ў малекулярным і іонным выглядзе;
- арганізаваць работу, накіраваную на фарміраванне даследчых уменняў вучняў;
- спрыяць фарміраванню ў вучняў лагічнага мыслення, умення хутка і якасна прымяняць атрыманыя веды на практыцы, развіваць навуковую мову вучняў;
- спрыяць выхаванню ў вучняў навукова абгрунтаванага ўспрымання навакольнага свету, самастойнасці меркаванняў, пачуццё адказнасці, уменняў працаваць у парах, групах, культуры хімічнага эксперыменту (правіл работы ў кабінеце хіміі).
Тып урока: урок замацавання і развіцця ведаў, уменняў, навыкаў.
Формы работы: франтальная, індывідуальная, парная, групавая.
Метады: - славесныя: гутарка, рассказ;
- наглядна-практычныя: дэманстрацыя доследаў, картачкі з
заданнямі;
- практычныя: лабараторны дослед.
Інтэрактыўны элемент урока – камп’ютарная прэзентацыя.
Абсталяванне і рэактывы:
- камп'ютар, праектар, экран, прэзентацыя ў “PowerPoint”;
- вучэбны дапаможнік: Шымановіч І. Я.Хімія. Падручнік для 8 класа ўстаноў агульнай сярэдняй адукацыі. – Мінск: Народная асвета, 2011;
- інструктыўныя карткі для правядзення лабараторнага доследу, «ацэначныя лісты вучня», дыягнастычныя матэрыялы па тэме «Рэакцыі іоннага абмену»(тэст));
- на сталах вучняў знаходзяцца: штатыў з прабіркамі, растворы фенолфталеіну, сернай кіслаты, гідраксіду калію і натрыю, сульфату калію, карбанату натрыю, саляная кіслата;
- на стале настаўніка знаходзяцца: штатыў з прабіркамі, крышталічныя карбанат натрыю і лімонная кіслата, растворы карбанату натрыю, лімоннай кіслаты, хларыду натрыю і гідраксіду калію.
Тэхналогія: элементы тэхналогіі праблемнага навучання, тэхналогіі развіваючага навучання, гульнявых тэхналогій.
Эпіграф урока: «Проста ведаць - яшчэ не ўсё, веды патрэбна ўмець выкарыстаць». І. В. Гётэ.
Ход урока
І.Арганізацыйны момант.
Мэта: забяспечыць знешнія абставіны і псіхалагічную падрыхтоўку да ўрока.
Псіхалагічны настрой на ўрок ствараем з дапамогай музычнага ўступлення (шум вадапада).
ІІ. Матывацыя.
Мэта: забяспечыць разуменне вучнямі мэты ўрока.
Настаўнік. Сёння мы прадоўжым вывучаць тэму “ Рэакцыі іоннага абмену”. (Слайд 1). Эпіграфам нашага ўрока з’яўляецца выказваннне «Проста ведаць - яшчэ не ўсё, веды патрэбна ўмець выкарыстаць». Гэтыя словы належаць І. В. Гётэ. (Слайд 2). Чаму іменна гэтае выказванне мы пакладзем у аснову нашага ўрока? Як вы думаеце? (Адказы вучняў).
Ну, а цяпер, зыходзячы з дэвіза ўрока і назвы тэмы разам вызначым мэты нашага ўрока. (Адказы вучняў).
ІІІ. Актуалізацыя і праверка ведаў.
Мэта: актуалізаваць суб’ектны вопыт вучняў, які спатрэбіцца ім пры раскрыцці тэмы.
Настаўнік. На мінулых уроках мы знаёміліся з тэорыяй электралітычнай дысацыяцыі, з рэакцыямі іоннага абмену, з умовамі працякання іонных рэакцый. Веды па пройдзеных тэмах спатрэбяцца нам на сёняшнім уроку. Таму спачатку правядзём размінку і паўторым асноўныя паняцці гэтых тэм.
У час урока вы будзеце весці «ацэначныя лісты», куды будзеце заносіць колькасць балаў, атрыманых пры выкананні розных заданняў)(Дадатак 1).
Размінка.
Заданне №1. «Хімічны трэнажор». (Слайд 3).
Закончы сказ адным словам. Вучні дабаўляюць у сказы патрэбныя словы.
1. Дадатна зараджаныя часцінкі - …(катыёны).
2. Адмоўна зараджаныя часцінкі - …(аніёны).
3. Рэчывы , водныя растворы або расплавы якіх праводзяць электрычны ток - …(электраліты).
4. Працэс распаду электралітаў на іоны пры растварэнні або расплаўленні рэчыва - ….(электралітычная дысацыяцыя).
5. Электраліты, пры дысацыяцыі якіх у водных растворах у якасці аніёнаў утвараюцца толькі гідраксід-іоны - …(асновы)
6. Электраліты, пры дысацыяцыі якіх у водных растворах у якасці катыёнаў утвараюцца толькі іоны вадароду - …(кіслоты).
7. Электраліты, пры дысацыяцыі якіх у водных растворах утвараюцца звычайна катыёны металаў і аніёны кіслотных астаткаў- …(солі).
8. Рэакцыі, якія адбываюцца ў водных растворах з удзелам іонаў электралітаў - …(іонныя рэакцыі).
Самакантроль. (За кожны правільны адказ пастаўце 1 бал, усяго за заданне - 8 балаў).
Заданне № 2. «Куча малая». (Слайд 4). На слайдзе беспарадкова запісаны формулы іонаў: Ca2+; K+; CI-; Mg2+; SO42-; CO32-; Fe3+; OH- . Размяркуйце іх па дзвюх папках з назвамі «КАТЫЁНЫ» і «АНІЁНЫ».
Узаемакантроль.(Слайд 5).( За правільна выкананае заданне пастаўце 1 бал).
Заданне 3. «Знайдзі мяне». (Слайд 6). Укажыце моцныя электраліты.
HCI; BaSO4; KOH; Ba(OH)2; Fe(OH)3; Na2CO3; Ca3(PO4)2 . Правяраем правільнасць выконвання задання.
Узаемакантроль. (Слайд 7). ( За правільна выкананае заданне пастаўце 1 бал).
Заданне 4. «Ау, электраліты! » . Напішыце ўраўненні дысацыяцыі ў водных растворах прапанаваных рэчываў у заданні №3. (Слайд 8). Адначасова каля дошкі працуе адзін вучань (рашае на адваротным баку дошкі). Аналізуем вынікі выканання задання.
Самаправерка.(Слайд 9). (За кожнае правільна састаўленае ўраўненне пастаўце 0,5 бала, усяго за заданне -2 балы).
IV. Сістэматызацыя, абагульненне ведаў.
Мэта: забяспечыць абагульненне і сістэматызацыю ведаў у вучняў пра рэакцыі іоннага абмену і ўмовы іх працякання, пра алгарытм састаўлення ўраўненняў рэакцый іоннага абмену.
Настаўнік. Давайце ўспомнім, якія рэакцыі называюцца рэакцыямі іоннага абмену? (Адказы вучняў). Рэчывы з якім тыпам сувязі можна аднесці да электралітаў? (Адказы вучняў). (Іонным – асновы, солі; кавалентным палярным – кіслоты). А цяпер ўспомнім, пры якіх умовах яны працякаюць. (Адказы вучняў).
Ствараем праблемную сітуацыю. Праводзім дэманстрацыйны дослед. Бяром крышталічныя карбанат натрыю і лімонную кіслату. Змешваем іх. Ці назіраем прыкметы рэакцый? Чаму? (Адказы вучняў). Што неабходна зрабіць для таго, каб рэакцыя адбылася? (Адказы вучняў). (Растварыць крышталічныя рэчывы. Іоны ў цвёрдых рэчывах знаходзяцца ў вузлах крышталічнай рашоткі і не могуць перамяшчацца свабодна, для таго каб абмяняцца іонамі, а ў растворы гэта становіцца магчымым). Праводзім рэакцыю паміж растворамі гэтых электралітаў. Якія прыкметы назіраем? (Адказы вучняў). (Вылучэнне газу).Значыць, рэакцыі паміж іонамі працякаюць у … (растворах) электралітаў і называюцца… (іоннымі рэакцыямі або рэакцыямі іоннага абмену (РІА)). Так як рэакцыі абмену працякаюць у растворах электралітаў, то і ўраўненні гэтых рэакцый будем запісваць у выглядзе іонаў(т. як рэакцыі працякаюць не паміж малекуламі , а паміж іонамі). І такія ўраўненні будуць называцца … (іоннымі). Успомнім парадак састаўлення ўраўненняў іонных рэакцый.(Адказы вучняў). Запрашаем да дошкі аднаго вучня. На прыкладзе ўзаемадзеяння салянай кіслаты і карбанату натрыю замацоўваем алгарытм састаўленя РІА: запіс малекулярнага ўраўнення, поўнага іоннага і іоннага скарочанага ўраўненняў рэакцыі.
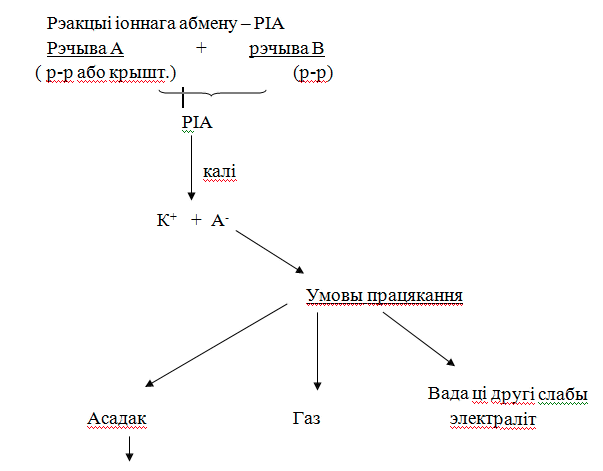
Ствараем наступную праблемную сітуацыю. Праводзім дэманстрацыйны дослед. Да раствору хларыду натрыю прыліваем раствор гідраксіду калію. Ці адбываецца гэтая рэакцыя? Чаму? (Адказы вучняў). ( Не назіраем прыкметы хімічных рэакцый? Няма пары катыёнаў і аніёнаў, якія могуць звязацца паміж сабой з утварэннем новага рэчыва, г.зн рэакцыя абарачальная, не ідзе да канца)). Запішам малекулярнае і поўнае іоннае ўраўненні гэтай рэакцыі. Пры якіх жа ўмовах працякаюць рэакцыі іонага абмену ў растворах электралітаў?(Адказы вучняў). ( Калі катыёны могуць звязацца з аніёнамі , г.зн. пры гэтым утвараецца асадак, газ або рэчывы, якія мала дысацыіруюць на іоны. Рэакцыя неабарачальная, г. зн. ідзе да канца). (На слайдзе дэманструецца схема-канспект пра рэакцыі іоннага абмену і ўмовы іх праходжання).(Слайд 10).(Дадатак 2).
А зараз мы пагуляем у гульню «Правер суседа». (Слайд 11). Работа ў парах.
Састаўце ўраўненні рэакцый ў малекулярным, поўным і скарочаным іонным выглядзе, укажыце ўмовы працякання хімічных рэакцый:
1 вучань: гідраксід калію + серная кіслата → …;
2 вучань: хларыд жалеза(ІІІ) + гідраксід калію → … .
Узаемаправерка( абмен сшыткамі). (Ключ для праверкі задання. (Слайд 12).). (За кожнае правільна састаўленае ўраўненне пастаўце 1 бал, усяго за заданне - 3 балы).
Наступная гульня - “Рэанімацыя”.(Слайд 13). Састаўце малекулярныя ўраўненні рэакцый, якія выражаны наступнымі скарочанымі іоннымі ўраўненнямі:
1 вучань : 2Н+ + CO32- → CO2 + Н2О ;
2 вучань: Cu2+ + 2OH- → Cu (OH )2 .
Узаемаправерка( абмен сшыткамі). (Ключ для праверкі задання. (Слайд 14).). (За правільна састаўленае ўраўненне пастаўце 1 бал).
V. Фізкультмінутка.
Мэта: стварыць умовы для зберажэння і захавання здароўя вучняў.
Гімнастыка для вачэй “Пальчык”. Прыцісніце палец да пераносіцы і паглядзіце на яго. Затым марудна адводзьце палец ад сябе, працягваючы сачыць за ім вачыма. Паўтарыце гэтае практыкаванне некалькі разоў.(Слайд 15).
VІ. Замацаванне ведаў.
Мэта: арганізаваць работу вучняў па прымяненню і замацаванню ведаў пра рэакцыі, якія адбываюцца ў растворах электралітаў і ўмовах іх праходжання на практыцы (з дапамогай хімічнага эксперымента) .
Настаўнік. Пры дапамозе чаго мы можам даведацца пра таямніцы, якія адбываюцца ў растворах электралітаў?(Адказы вучняў).( Хімічнага эксперымента).
Так, зараз пераходзім да практычнай часткі ўрока, эпіграфам да якой стануць словы Д.І.Мендзялеева “ Дослед – найкарацейшы шлях да пазнання сапраўднасці”. (Слайд 16).Як вы думаеце, чаму пад такім эпіграфам мы будзем працаваць? (Адказы вучняў). Вам неабходна правесці наступны лабараторны дослед, у выніку якога вы павінны даказаць, што пры дадзеных умовах рэакцыі іоннага абмену ідуць да канца, з’яўляюцца абарачальнымі.
Работа ў групах(па 4-5 вучняў). Праводзіцца навучанне правілам бяспекі пры рабоце : з растворамі кіслот, шчолачаў і солей; са шкляным посудам. Вучні працуюць па інструктыўных картачках.(Дадатак 3). Ад кожнай групы адзін вучань дакладвае аб выніках праведзенага доследу, робіць вывады. Справаздачу аб праведзеных доследах афармляюць у наступнай табліцы.( Слайд 17).
|
Выкананне доследу (рысунак)
|
Назіранні
|
Ураўненні рэакцый, вывад
|
|
|
|
|
Самакантроль. (За правільна выкананае эксперыментальнае заданне пастаўце 4 балы: 3 балы за ўраўненні рэакцый і 1 бал – за вывад).(Слайд 18).
VІІ. Кантроль засвоеных ведаў.
Мэта: выявіць якасць і ўзровень засваення ведаў вучнямі; выявіць недахопы і правесці карэкцыю выяўленых прабелаў у ведах вучняў.
Правядзенне тэставай работы. (Дадатак 4).
Узаемаправерка. (Слайд 19).(За кожны правільны адказ пастаўце 1 бал, усяго за тэст -10 балаў ).
VІІІ. Дамашняе заданне.
Мэта: забяспечыць разуменне вучнямі мэты, зместу і спосабаў выканання дамашняга задання.
Настаўнік дае кароткі інструктаж па выконванню дамашняга задання.
§ 33, заданні 6,10.(Слайд 20).
ІХ. Рэфлексія.
Мэта: стварыць сітуацыю рэфлексіі па прычыне ўсведамлення вучнямі сябе ў дзейнасці, якую яны выконвалі.
У пачатку ўрока вашай увазе былі прапанаваны гукі вадападу. Як гэта звязана з нашай тэмай урока? (Адказы вучняў).
Як вы лічыце, ці дасягнулі вы мэты ўрока? (Адказы вучняў).
Ці вызвала тэма ўрока цікавасць? (Адказы вучняў).
Як вы думаеце, ці спатрэбіцца вам гэта ў жыцці? (Адказы вучняў).
Падлічыце свае балы ў лісце “самаацэнкі” і з дапамогай шкалы выстаўце сабе адзнаку ў сшытках і здайце іх мне для выстаўлення адзнак у журнал.
Малайцы, вы сёння добра папрацавалі і паказалі нядрэнныя веды, асабліва пры правядзенні практычнай часткі ўрока.
А цяпер адзначце свой стан і настрой пасля праведзенага ўрока на “дрэве стану”. Уважліва разгледзьце малюнак і абвядзіце таго чалавечка, кім вы сябе адчуваеце пасля нашага ўрока .(Слайд 21).
Дзякуй вам за ўрок! Да пабачэння!(Дадатак 5).(Слайд 22).
Дадатак 1
«Ацэначны ліст вучня»
|
Назвы заданняў
|
Інструкцыя па ацэньванню заданняў
|
Колькасць балаў, якія набраў вучань
|
|
«Хімічны трэнажор»
|
За кожны правільны адказ пастаўце 1 бал, усяго за заданне - 8 балаў
|
|
|
«Куча малая»
|
За правільна выкананае заданне пастаўце 1 бал
|
|
|
«Знайдзі мяне»
|
За правільна выкананае заданне пастаўце 1 бал
|
|
|
«Ау, электраліты!»
|
За кожнае правільна састаўленае ўраўненне пастаўце 0,5 бала, усяго за заданне -2 балы
|
|
|
«Правер суседа»
|
За кожнае правільна састаўленае ўраўненне пастаўце 1 бал, усяго за заданне - 3 балы
|
|
|
«Рэанімацыя”
|
За правільна састаўленае ўраўненне пастаўце 1 бал
|
|
|
Хімічны эксперымент
|
За правільна выкананае эксперыментальнае заданне пастаўце 4 балы: 3 балы за ўраўненні рэакцый і 1 бал – за вывад
|
|
|
Тэставая работа
|
За кожны правільны адказ на пытанне тэста пастаўце 1 бал, усяго за тэст -10 балаў
|
|
Падлічыце агульную колькасць балаў і згодна наступнай табліцы пастаўце сабе адзнаку за ўрок
|
Колькасць балаў атрыманых на ўроку
|
Адзнака за вучэбную дзейнасць на ўроку
|
|
1
|
1
|
|
2
|
2
|
|
3—5
|
3
|
|
6—8
|
4
|
|
9—11
|
5
|
|
12—14
|
6
|
|
15—18
|
7
|
|
19—23
|
8
|
|
24—28
|
9
|
|
29—30
|
10
|
Мая адзнака за ўрок : __
Дадатак 2
Схема-канспект “Рэакцыі іоннага абмену”
CuSO4 + 2КOH →Cu(OH)2 + К2SO4 малекулярнае ўраўненне
Cu2+ + SO42- + 2К+ + 2OH- → Cu(OH)2 + 2К+ + SO42- поўнае іоннае ўраўненне
Cu2+ +2OH- → Cu(OH)2 скарочанае іоннае ўраўненне
Увага! Пры запісах іонных ураўненняў рэакцый карыстайцеся табліцай растваральнасці.
Дадатак 3
Інструктыўныя картачкі да лабараторнага доследу
Заданне для першай групы.
Да 1-2 мл раствору гідраксіду калію дабаўце некалькі кропель фенолфталеіну( што назіраеце?), а затым да атрыманага раствору прыліце прыкладна 1 мл салянай кіслаты. Адзначце прыкметы рэакцый. Састаўце ўраўненне рэакцыі нейтралізацыі ў малекулярным, поўным і скарочаным іонным выглядзе. Зрабіце вывад.
Заданне для другой групы.
Да раствору сульфату медзі(ІІ) аб'ёмам прыкладна 1 мл дабаўце некалькі кропель раствору гідраксіду натрыю. Якія прыкметы назіраеце? Састаўце ўраўненне рэакцыі ў малекулярным, поўным і скарочаным іонным выглядзе. Зрабіце вывад.
Заданне для трэцяй групы.
Да1-2мл раствору карбанату натрыю дабаўце прыкладна 1 мл раствору салянай кіслаты. Якія прыкметы назіраеце? Састаўце ўраўненне рэакцыі ў малекулярным, поўным і скарочаным іонным выглядзе.Зрабіце вывад.
Заданне для чацвёртай группы.
Да1 -2 мл раствору хларыду натрыю прыліце такі ж аб'ём сульфату калію. Ці назіраеце прыкметы хімічнай рэакцыі? Састаўце ўраўненне рэакцыі ў малекулярным, поўным іонным выглядзе. Зрабіце вывад.
Дадатак 4
Тэставая работа
1. Якія з пералічаных ніжэй рэчываў могуць утварыцца ў ходзе рэакцый іоннага абмену? а) Na3PO4; б) Fe(OH)3 ; в) H2O ; г) KOH .
2. Газ выдзяляецца ў выніку ўзаемадзеяння іонаў:
а) Ba2+ і CO32− ; б) 2Н+ і СО32− ; в) Н+ і ОН−; г) СО32− і Са2+.
3. Могуць адначасова знаходзіцца ў растворы іоны:
а) Al3+ і PO43−; б) Na+ і NO3−; в) K+ і ОН−; г) Ag+ і Cl−.
4. Правая частка ўраўнення дысацыяцыі сульфату медзі(II):
а)Cu + SO3; б) Cu2++ SO42-; в)2Cu++ SO42-; г)Cu2+ + SO32- .
5.Сутнасць рэакцыі паміж сульфатам жалеза(ІІ) і гідраксідам натрыю паказваецца скарочаным іонным ураўненнем:
а) Fe2+ + 2ОН- = Fe(OH)2;
б) Fe3+ + ЗОН- = Fe(OH)3;
в)2Na+ + S042- = Na2S04;
г) FeS04 + 2Na+ + 2ОH- = Fe(OH)2 + 2Na+ + SO42-.
6. Скарочанае іоннае ўраўненне Ba2+ + SO42- → BaSO4↓ адпавядае наступнаму малекулярнаму ўраўненню:
а) Ba + H2SO4 → BaSO4 + H2;
б) BaO + SO3 → BaSO4 ;
в) BaCl2 + K2SO4 → BaSO4 + 2KCl;
г) BaO + H2SO4 → BaSO4 + H2O.
- З выдзяленнем газу працякае рэакцыя паміж растворамі:
а) нітрату серебра(І) і салянай кіслаты;
б) карбанату барыюі гідраксіду кальцыю;
в) сульфату калію і сернай кіслаты;
г) сульфіду натрыю і салянай кіслаты.
8. З выпадзеннем асадку працякае рэакцыя паміж растворамі:
а) сульфату калію і салянай кіслаты;
б) нітрату серабра(І) і хларыду натрыю;
в) гідраксіду калію і сернай кіслаты;
г) хларыду натрыю і салянай кіслаты.
9.Устанавіце адпаведнасць паміж зыходнымі рэчывамі і скарочаным іонным ураўненнем:
|
зыходныя рэчывы
|
іоннае ўраўненне
|
|
А. Al2O3 + H2SO4 →
Б. Al2(SO4)3 + KOH →
В. Al(OH)3 + H2SO4 →
|
1) Al3+ + 3OH- → Al(OH)3↓
2) H+ + OH- → H2O
3) 2K+ + SO42- → K2SO4
4) Al2O3 + 6H+ → 2Al3+ +3H2O
5) Al(OH)3 + 3H+ → Al3+ +3H2O.
|
10. Прыкметай рэакцыі паміж гідраксідам медзі(ІІ) і гідраксідам натрыю з’яўляецца:а) з’яўленне паху; б) утварэнне блакітнага асадку;
в) выдзяленне газу; г) выпадзенне асадку.
Дадатак 5
Рэфлексія “Дрэва стану”
разгарнуць » / « згарнуць